Témata k prostudování:
Definice pojmů: eupnoe, tachypnoe, bradypnoe, hyperventilace, hypoventilace, dyspnoe, ortopnoe, apnoe, hyperpnoe, hypopnoe. Definice objemů plicních: dechový objem, inspirační a expirační rezervní objem, vitální kapacita, jednosekundová vitální kapacita (FEV1), inspirační a expirační kapacita, celková kapacita plic, funkční reziduální kapacita, reziduální objem. Ventilace (klidová, maximální), dechová rezerva. Mrtvý prostor anatomický vs. funkční. Vazba kyslíku na hemoglobin, disociační křivka. Saturace krve kyslíkem (SpO2). Transport CO2 v krvi. Definice pojmů: parciální tlak, hypoxie, hyperkapnie. Možné příčiny hypoxie – hypoxie hypoxická, transportní (anemická), ischemická (stagnační, cirkulační), histotoxická. Chemoreceptory důležité pro regulaci dýchání – centrální vs. periferní, jejich umístění a citlivost k změnám pCO2/pH a pO2.
![]()
Dechový objem je objem jednoho vdechu- tedy to, co nadechneme V KLIDU, asi půl litru. Počítáme sem také anatomický mrtvý prostor, kde neprobíhá výměna plynů – to je asi 150 ml. Víc si o tom povíme později.
![]()
Po normálním (klidovém) výdechu můžeme ještě vydechnout nějaký vzduch “na sílu”, tomu říkáme rezervní expirační objem, protože jde o takovou rezervu, která nám zbyde i po běžném výdechu (expiriu). ERV = 1,7 l.
![]()
Stejně jako máme rezervu u výdechu, máme ji i u nádechu a nazýváme ji rezervní inspirační objem – jde tedy o vzduch, který můžeme nadechnout ještě po běžném nádechu. IRV = 3 l.
I přes naši veškerou snahu nejsme schopní úplně vyprázdnit plíce. Vždy v nich zůstane asi 1,3 l vzduchu. Tomuto objemu se pak říká reziduální objem (RV). Jinak by alveoly měly tendenci kolabovat.
Malé upozornění: Objemy musíte umět. K testu, ke zkoušce, i do dalších ročníků. Mají velkou roli v diagnostice

Teď se podíváme na kapacity a budeme muset trochu sčítat, ale když se budete držet synchronizovaných barev a obrázků, určitě nakonec pochopíte!
![]()
Vitální kapacita (značena VC) jsou všechny předešlé objemy dohromady – dechový, inspirační rezervní a expirační rezervní objem, tedy vzduch, který maximálně vydechneme po maximálním nádechu.
![]()
Objem normálního nádechu + rezervní inspirační objem. (Nadechneme se klidově a pak ještě na sílu).
![]()
Objem normálního výdechu + rezervní expirační objem. (Vydechneme normálně a pak ještě na sílu).
![]()
Je to součet objemu vitální kapacity a reziduálního objemu. Tedy jinak řečeno úplně celková kapacita.
![]()
Jedná se o objem vzduchu, který zůstane v plicích po volném výdechu.

![]()
Jde o objem vzduchu, který vydechneme během první sekundy usilovného výdechu. Takže vy se nadechnete maximálně a pak co nejrychleji, nejprudčeji vydechnete. Nejde vám to? Pravděpodobně vám diagnostikují nějakou obstrukční poruchu. Proč? Protože vy to množství vydechnete, jen vám to trvá dýl. Je tam třeba překážka. Co znamená 1? Že je to v 1. sekundě. Kdyby tam bylo FEV2 je to ve 2. sekundě.
FVC je naopak usilovná vitální kapacita. Je to další kapacita, co se měří u vyšetření. Je to kolik dokážete vydechnout po tom, co jste se maximálně nadechli. Pokud vám to nejde, většinou půjde o restrikční poruchu. Proč restrikce? Protože na rozdíl od té FEV1. Vy vydechnete méně vzduchu, než průměrný člověk. Jako by tam chyběla ta funkční plicní tkáň.
Na co je to dobré? Diagnostika!! Používáme tzv,. Tiffeneaův index, kdy je to prostě a jednoduše zlomek. Do čitatele hodíte naměřené FEV1 a do jmenovatele FVC (FEV1/FVC). Průměrný zdravý člověk se bude pohybovat s výsledkem okolo 80%.
Nezapomeňte, že všechny poruchy jsou více či méně kombinované. To platí u všeho. Jen vzádně najdete jen jednu čistou poruchu.
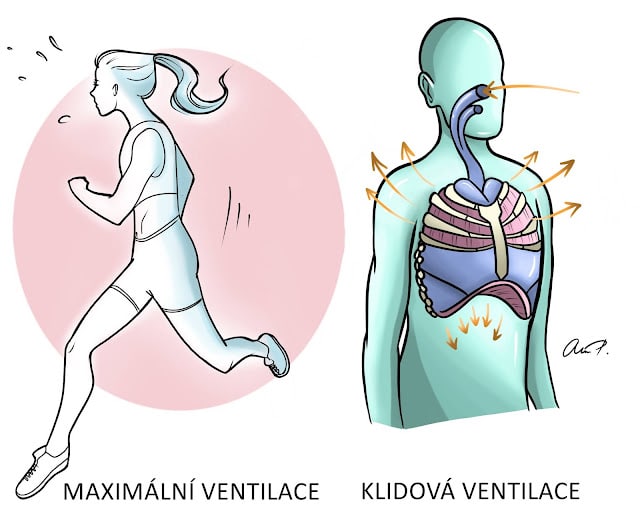
Klidová ventilace
Klidová ventilace je vlastně dýchání v klidu. Za takovou minutu v klidu stihneme asi 16 dechů. Při zátěži se pak naše dýchání zrychluje. Prvně bude docházet k prohloubení dechu a později právě i k zvýšení frekvence.
Maximální ventilace
Maximální ventilace je vlastně nejusilovnější dýchání. Vztaženo na jednotku času, můžeme se při maximální ventilaci pohybovat v rozmezí 90-160 litrů vzduchu za minutu, záleží na trénovanosti osoby. Já třeba mám maximálku při dobíhání na zastávku.
Dechová rezerva
Při dechové rezervě mluvíme o poměru minutové ventilace a maximální minutové ventilace, tedy o tom kolikrát jsme schopni zvýšit objem dýchaného vzduchu – proto také název rezerva.
Mrtvý prostor anatomický vs. funkční.
Definice mrtvého prostoru je: celkový objem vzduchu (v konduktivní oblasti dýchacích cest) kde neprobíhá výměna plynů s krví.
Aby se tento údaj dal uplatnit v klinice, rozlišujeme 2 podtypy tohoto objemu a to anatomický a funkční. Anatomický mrtvý prostor je ve své podstatě objem dýchacích cest, tedy objem vzduchu, který se po nádechu ještě nesmísil s alveolárním vzduchem. Dýchací cesty jsou ta část dýchací soustavy, kudy proudí vzduch dovnitř při nádechu a ven při výdechu, ale která se nepodílí na výměně dýchacích plynů ještě. Anatomický mrtvý prostor představuje 150-200 ml.
Funkční (také fyziologický) mrtvý prostor je, rovněž jako anatomický mrtvý prostor, objem, ve kterém dochází k výměně dýchacích plynů, ale zahrnuje i neprokrvené alveoly. U zdravého člověka tedy předpokládáme, že jeho funkční MP se bude rovnat anatomickému mrtvý prostor. Měření mrtvého prostoru se provádí dusíkovým testem (hluboký nádech kyslíku a následný pomalý výdech, ve kterém monitorujeme koncentraci dusíku).

Vazba kyslíku na hemoglobin, disociační křivka.
Dýchací plyny jsou v organismu transportovány krví. Je však třeba si uvědomit, že spotřeba O2 a tvorba CO2 v organismu je mnohem vyšší než množství, které se v krvi fyzikálně rozpustí. Abychom tedy dokázali tělu dodat dostatečné množství O2 a odstranili CO2, musíme mít i jiné způsoby transportu. Nejvýznamnějšími jsou vazba O2 na hemoglobin a přeměna CO2 na HCO3-. Vedle toho si však musíme uvědomit, že oba plyny jsou v krvi fyzikálně rozpuštěné a CO2 se kromě formy HCO3- přenáší také i ve vazbě na hemoglobin.
Jak je kyslík na hemoglobin navázaný? Hemoglobin (Hb) je alosterický metaloprotein s tetramerní strukturou. Představíme si ho jako molekulu složenou ze 4 bílkovinných řetězců (globinu) na který (každý jeden) je navázáno hemové jádro (komplex porfyrinu a Fe 2+ molekuly). Každý atom Fe může reverzibilně vázat molekulu kyslíku O2. Množství O2, které se naváže na Hb, závisí od parciálního tlaku kyslíku v krvi. Závislost navázaného množství O2 na parciálním tlaku je vyjádřena disociační (saturační, vazebnou) křivkou.
Disociační křivka má sigmoidní tvar a můžeme na ní popsat určité fenomény. Od hodnoty parciálního tlaku 0-10 mmHg stoupá křivka jen mírně. Je to proto, že s postupným navazování molekul O2 dochází i ke konformačním změnám na Hb, čímž se zvýší jeho afinita k O2. Proto bude křivka v rozmezí 10-40 mmHg stoupat strmě. Strmost se postupně snižuje a od hodnoty 90 mmHg je více méně saturovaná – všechen Hb je kyslíkem nasycený. Tento průběh křivky má své výhody.
Za 1. jak jsme se již dozvěděli, krev je plně nasycena kyslíkem při 90 mmHg, to znamená, že při jakémkoliv malém výkyvu parciálního tlaku kyslíku v alveolu (který je okolo 100 mmHg) je krev stále plně saturovaná.
Za 2. kyslik se bude z Hb nejlépe uvolňovat pokud parciální tlak kyslíku bude pod 40mmHg, což je přibližná hodnota parciálního tlaku ve tkáni – tedy na základě faktu, že je v úseku 10-40mmHg disociační křivka strmá, můžeme říci, že tkáním stačí malý rozdíl parciálního tlaku na to, aby se uvolnilo relativně velké množství kyslíku.
Abychom to měli kompletní, je na místě zmínit i to, že neznáme pouze jeden druh Hb. Existuje hned několik typů a navzájem se liší pořadím aminokyselin v řetězci, tedy i svou afinitou ke kyslíku. Globinové řetězce označujeme řeckou abecedou a jelikož jde o tetramer, jsou dohromady 4. U dospělých najdeme v největším množství HbA. U novorozenců se nachází speciální HbF (fetální), který se vyznačuje vyšší afinitou ke kyslíku a umožňuje tak u plodu odebírat přes placentární bariéru kyslík z HbA matky bez přímého kontaktu jejich krví. Kromě zmíněných existují ještě další druhy hemoglobinu jako například HbA2 …
Saturace krve kyslíkem (SpO2).
Saturace, tedy nasycení krve kyslíkem, se znázorňuje tzv. saturační křivkou, kterou jsme diskutovali výše. Samotná saturace se však nemění jen s parciálním tlakem, je to dáno tím, že Hb má složitou strukturu, která této molekule dovoluje se změnit v závislosti na teplotě a na základě vazby různých ligandů na různých místech. Jedná se hlavně o molekuly O2, CO2, H + (ovlivňuje pH), BPG (2,3-bisfosfoglycerát) je molekula, která vzniká glykolýzou v erytrocytech a ukládá se mezi β řetězce Hb, což stabilizuje molekulu Hb v deoxygenovaném stavu. Právě tato vlastnost propůjčuje Hb výhodu při zásobování metabolicky aktivních tkání kyslíkem – jestliže je tkáň metabolicky aktivní, stoupá v ní teplota, produkuje se CO2 jako konečný produkt metabolismu, stoupá koncentrace H + (snižuje se pH) a produkuje se také BPG.
Všechny tyto stimuly snižují schopnost Hb navázat kyslík a posouvají tak disociační křivku doprava. Pokud je situace opačná, tedy máme více O2 než CO2, vyšší pH, nižší hladinu BPG a nižší teplotu, popisujeme prakticky situaci v alveolárních kapilárách, schopnost Hb vázat kyslík zvýší a disociační křivka se posouvá směrem doleva.
Posun křivky doprava na základě zvýšeného parciálního tlaku CO2 a sníženého pH se nazývá také Bohrův efekt (nese jméno podle Christiana Bohra, otce Nielse Bohra, který vymyslel Bohrův model atomu – některý rodiny jsou úspěšný a některý čumí na netflix). Kromě tohoto efektu také jako první popsal mrtvý prostor.
Transport CO2 v krvi.
Jak jsme již uvedli výše, CO2 je transportováno v krvi majoritně ve formě HCO3-. V buňkách tato molekula (CO2) vzniká jako produkt energetického metabolismu a je procesem difúze uvolňována ve směru gradientu parciálního tlaku do cév. Část z něj se v krvi rozpustí, avšak toto množství je velmi malé ve srovnání s tím, které potřebujeme reálně z těla transportovat ven. Abychom v těle dokázali vytvořit z molekuly CO2 molekulu HCO3-, je potřebný enzym karboanhydráza, který se nachazí pouze v erytrocytech. Kromě toho se CO2 může v krvi transportovat i ve vazbě na bílkovinnou část Hb (-> tzv. karbaminohemoglobin).
Jak se tedy z CO2 stává HCO3- a zase CO2? CO2, který byl z tkání vyloučen po svém gradientu parciálního tlaku do krve, se z plazmy do erytrocytů dostává stejným způsobem. V erytrocytech se působením karboanhydrázy (+ H2O) mění na H2CO3, který disociuje na H + a HCO3-. Proton ve formě H + je pufrovaný Hb (vzniká Hb-H) a HCO3- prochází difúzí do plazmy výměnou za Cl-. Tento sled událostí se děje na periferii. Naopak v plicích, kde chceme CO2 předat, dochází k úplně opačnému ději.
Výměna iontů Cl- za HCO3- se jmenuje i chloridový posun (chloride shift) nebo podle svého objevitele Hamburgerův efekt.
Možná by bylo fajn, připomenou si některé důležité pojmy.
Co je to parciální tlak?
Vzduch je směs plynů, které se nacházejí kolem nás a tvoří atmosféru. Na vzduch působí síla gravitace a zároveň vzájemné působení molekul, které vyvolávají atmosférický tlak 760 mmHg. Nakolik je vzduch tvořen z více plynů, každý plyn má svůj tlak – parciální tlak, který odvodíme od jejich procentuálního zastoupení ve vzduchu (tedy kyslíku je zhruba 21%, tedy 760×0,21 = 160 mmHg).
Co je to hypoxie?
Je to souhrnný název pro nedostatek kyslíku v těle nebo v jednotlivých tkáních. Pozor, neplést s hypoxémií! Ta odkazuje na nedostatek kyslíku přímo v arteriální krvi!
Dalším termínem, který se vztahuje ke kyslíku, je anoxie, tento termín značí naprostý nedostatek kyslíku.
Jaké známe příčiny hypoxie?
Hypoxická hypoxie se fyziologicky vyskytuje při pobytu ve vyšších nadmořských výškách, ale může se objevit i patologická, a to při hyperventilací při plicních, či nervosvalových nemocech.
Transportní (anemická) – objevuje se když je v těle omezen transport kyslíku, to znamená ztráta krve, anémie, otrava CO.
Ischemická (stagnační, cirkulační) – objevuje se při omezeném průtoku krve tkáněmi (srdečně selhání, uzavření tepen, šokové stavy).
Histotoxická – nastává, když buňky z nějakého důvodu nedokáží kyslík využít (např. otrava kyanidem, kdy dochází k poškození dýchacího řetězce).
Co je to hyperkapnie?
Je to zvýšení koncentrace CO2 v krvi nebo ve tkáních, které je způsobeno retencí (zadržením) CO2 v těle. Příčinou může být také nedostatečná výměna plynů v alveolech.
Další, co má na respirační systém velký vliv jsou chemoreceptory.
Chemoreceptory jsou důležité pro regulaci dýchání. Dělíme je na centrální a periferní chemoreceptory. Nejvíce se liší jejich umístěním a citlivostí ke změnám pCO2/pH a pO2.
Centrální chemoreceptory nacházíme pod povrchem prodloužené míchy. Tyto chemoreceptory reagují hlavně na vzestup CO2 a H+. CO2 dokáže bez problémů projít přes hematoencefalickou bariéru, kdežto H+ a HCO3- procházejí obtížně. CO2 tedy vstupuje do mozku a zde je hydratován na H2CO3 a dále disociován na H+ a HCO3-. Tím pádem se zvýší koncentrace H+ a dýchací centrum zareaguje tak, že zrychlí dýchání (hyperventilace).


Mezi periferní chemoreceptory řadíme glomus caroticum a glomus aorticum (Představte si prostě senzory v oblouku aorty a na bifurkaci karotidy). Tato tělíska jsou hojně zásobována krví a jsou citlivá zejména na pokles rozpuštěného kyslíku v krvi. Proč na rozpuštěný kyslík? Protože jsou právě vyživována tím rozpuštěným kyslíkem. Takže logicky poznají, když ho nemají. Na hypoxii reagují dříve, než centrální chemoreceptory, ale nemají ten efekt takt dlouhý. Jak zareagují? Vyšlou signál, aby se zvedla hloubka dechu a taky zrychlila frekvence, jakou člověk dýchá. Shodneme se na tom, že když začne člověk dýchat rychleji, bude vydechovat více CO2. CO2 je kyselé (acidifikující), takže se zbavujeme kyselé složky a pH se vyrovnává. Toto se stane vždy, když je nižší pO2, vyšší pCO2.
Nechápeš mechanismy kolem přeměny CO2, H+ a HCO3-?
Doporučuju článek Acidobazická rovnováha 1.část
Potřebuješ si víc ujasnit chemoreceptory?
Zkus se podívat na článek Acidobazická rovnováha 2.část
Autoři: Marie Tormová, Ján Tkáč